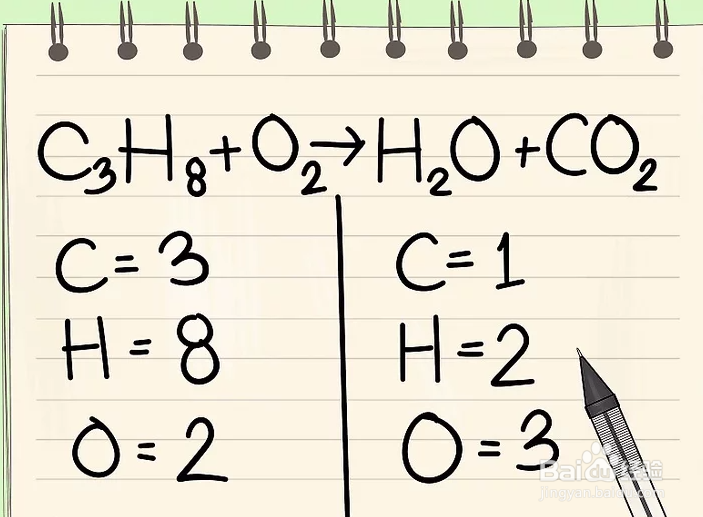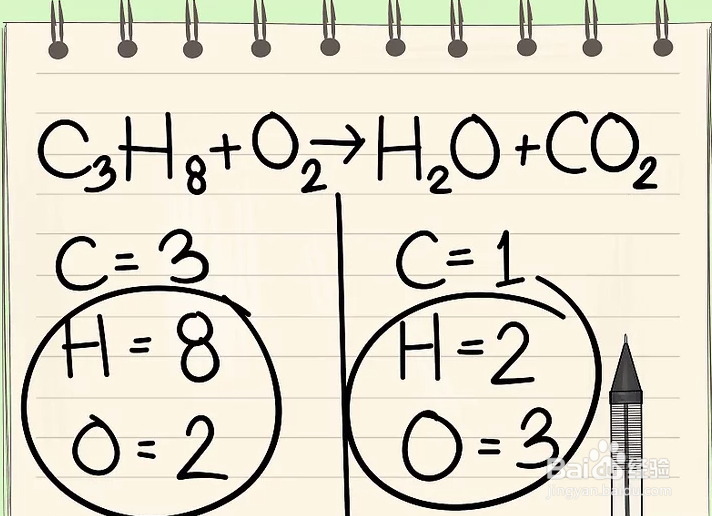1、我们使用传统配法写出已有的化学方程式。我们就拿下面的方程式举例:C3H8+ O2--> H2O + CO2。在这个反应中,丙烷(C3H8) 在氧气中被点燃,生成水和二氧化碳。
2、分别写出化学方程式左右两边每一个原子的个数。通过观察方程式中每个原子的下角标得知每个原子的个数,计算程式两边各原子的总数,并写下来。左边:3个碳,8个氢,2个氧右边:1个碳,2个氢,3个氧
3、记住:最后再配平氢原子和氧原子。这就意味着你需要先配平碳原子。
4、给方程式右边的单个碳原子加一个系数3,这样右边的碳原子数就与左边的碳原子数配平了。C3H8+ O2--> H2O +3CO2右边方程式中碳原子的系数3与左边方程式中碳原子的下脚标3,都意味着有3个碳原子。在化学方程式中,系数可以调整,但脚标数不能变动。
5、接着,配平氢原子。右边方程式中有8个氢原子,所以左边方程式中也需要8个氢原子。C3H8+ O2--媪青怍牙>4H2O + 3CO2在右边方程式中,氢原子的脚标为2,也就是说已经有2个氢原子了,所以我们只需加一个系数4就可以得到8个氢原子。氢原子数等于脚标数2乘以系数4,也就等于8,也就是左边氢的数量。
6、其余6个氧来自于三个CO2。(3 x 2 = 6 个氧 + 其余的 4 = 10)
7、将氧原子数配平,我们就大功告成了!由由于我们给右边的方程式中的分子加了系数,因而氧原子的数目变了。方程式右边的水分子中有4个氧原子,而二氧化碳分子中有6个氧原子,也就是说右边方程式中一共有10个氧原子。给右边的方程式中的氧分子前加一个系数4,这样两边就都有10个氧分子了。C3H8+5O2--> 4H2O + 3CO2.现在,碳分子、氢分子和氧分子的数目都被配平了。化学方程式完成!