C=1000*P(密俣觊鄄幼度)*w(质量分数)/M(该物质的摩尔质量)。
物质的量浓度:单位体积溶液所含溶质的物质的量,叫做溶质的物质的量浓度。
换算柬缰缣挞公式及推导公式:
1、把单位体积设为1L=1000ml(换算单位是因为和密度单位统一)
2、物质的量浓度的基本公式是c=n/V,在这里的n表示的是溶质的物质的量,V表示溶液的体积
那么根据n(溶质的物质的量)=m/M,且m(溶质的质量)=ρv
3、溶质的质量=溶液的体积×溶质的百分比, 所以可以得到,m(溶质的质量)=ρv=ρ×1000ml×w
4、把这个带进去n(溶质的物质的量)=m/M,得到n=ρ×1000ml×w/M
5、最后带进去c=n/V,得到c=ρ×1000ml×w/M×1L。
扩展资料:
注意
1、物质的量浓度公式中的体积是指溶液的体积,而不是溶剂的体积。
2、在一定物质的量浓度溶液中取出任意体积的溶液,其浓度不变,但所含溶质的物质的量或质量因体积的不同而不同。
3、溶质可以是单质、化合物,也可以是离子或其他特定组合。如 C(Cl2)=0.1mol/L C(NaCl)=0.2mol/L C(Fe)
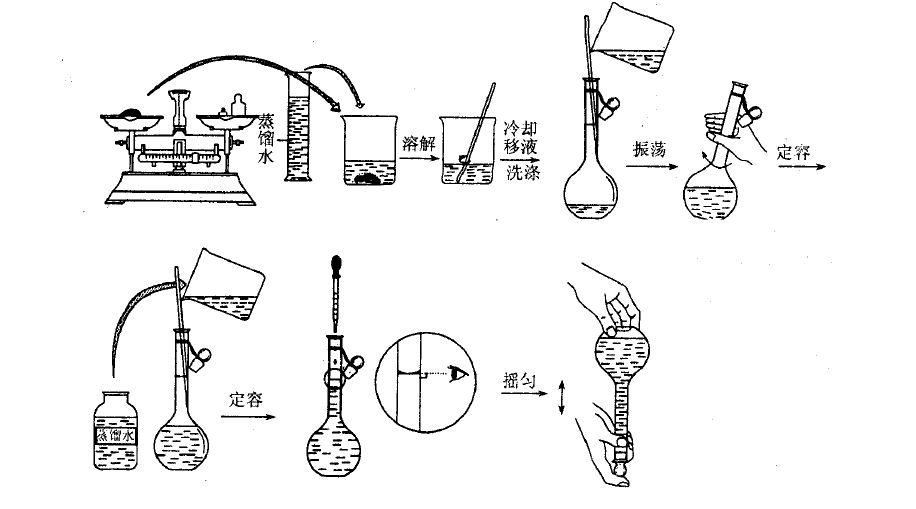
4、溶质的量是用物质的量来表示的,不能用物质的质量来表示。例如:配制1mol/L的氯化钠溶液时,氯化钠的相对分子量为23+35.5=58.5,故称取58.5g氯化钠,加水溶解,定容至1000ml即可获得1mol/L的氯化钠溶液
5、带结晶水的物质作溶质时,溶质是结晶水合物中除去结晶水剩下的部分。
参考资料来源:百度百科——质量分数