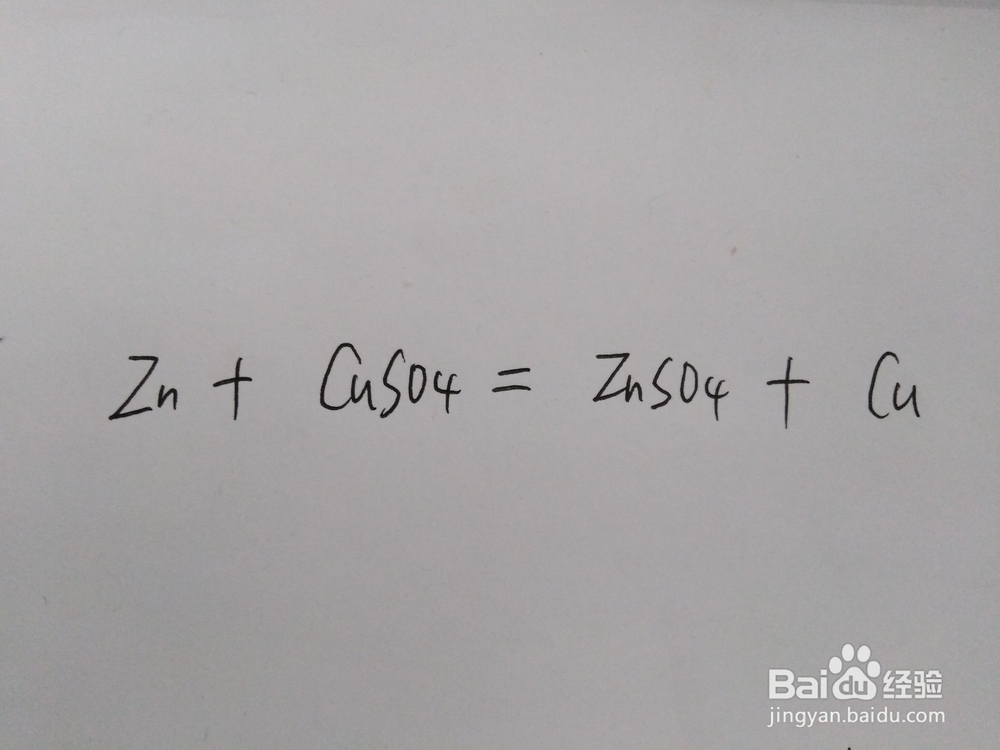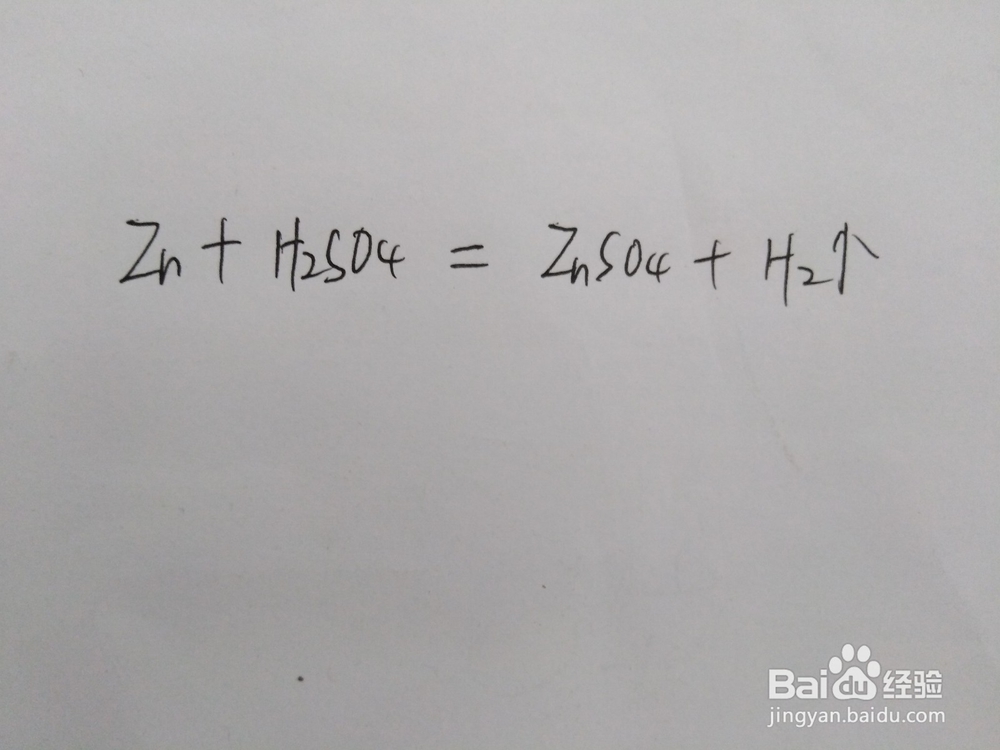1、首先回顾涉及到的知识点一:金属的还原性顺序,如下图:确认两点:1、锌的还原性比铜强;2、Cu的还原性顺序在(H)之后。
2、高中化学还学到的一个,原电池反应;最典型的原电池反应就是铜锌原电池,利用的原理当然还是锌的还原性比铜强。
3、另外基于Cu的还原性在(H)之后得到的一个结论:Cu与稀盐酸与稀硫酸不反应。Cu与浓硫酸可以反应,利用的知识是:浓硫酸具有强氧化性。
4、基于以上的所有知识点,下面来解决这个分离的问题:首先向溶液中加入过量的锌粉,用于置换溶液中的Cu,反应方程式如下图
5、溶液中生成的沉淀,有置换出来的Cu,还有过量的锌粉,可以通过过滤进行分离,此时溶液中只有硫酸锌了,就实现了分离。
6、如果不过滤沉淀,可以向溶液中再加入过量的稀硫酸,使锌粉与稀硫酸反应再次生成硫酸锌,反应式如下图
7、基于铜无法与稀硫酸反应,在加入过量锌粉又加入过量稀硫酸的情况下,溶液中不再含有硫酸铜,如有需要,可将过滤出的铜,与浓硫酸反应生成硫酸铜,注意会生成二氧化硫气体。